نیتروژن با اینکه بعد از فلور و اکسیژن بیشترین الکترونگاتیوی را دارد اما بدلیل پیوند سه گانه مستحکم بین دو اتم آن N≡N غیر فعال است. انرژی لازم برای شکستن پیوند 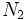 cal/mol 225 است. به همین دلیل نیتروژن موجود در هوا مولکول بیاثری است. نیتروژن هوا فقط بر فلز لیتیم اثر کرده و یک ترکیب غیر استوکیومتری ایجاد میکند. اغلب واکنشهای نیتروژن در دماهای بالا انجام میگیرد.
cal/mol 225 است. به همین دلیل نیتروژن موجود در هوا مولکول بیاثری است. نیتروژن هوا فقط بر فلز لیتیم اثر کرده و یک ترکیب غیر استوکیومتری ایجاد میکند. اغلب واکنشهای نیتروژن در دماهای بالا انجام میگیرد.
نیتروژن در دماهای بالا با اکثر فلزات و غیر فلزات ترکیب شده و ترکیباتی به نام نیترید ایجاد می کند. در نیتریدها اتم نیتروژن حالت اکسایش (3-) دارد. نیترید فلزات قلیایی بجز لیتیم به روش غیر مستقیم تهیه میشود. نیتروژن با فلزات قلیایی خاکی هم ترکیب شده و نیتریدهایی به فرمول 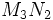 ایجاد میکند.
ایجاد میکند.
ترکیب نیتروژن با عناصر گروه سوم مانند بور و آلومینیوم ترکیبات سختی ایجاد میکند. بور نیترید در دماهای بالا و فشار زیاد ساختاری مانند ساختار الماس پیدا میکند و سختی آن بیشتر از الماس است. نیتریدهای فلزات واسطه بخاطر رسانایی خوب جریان الکتریکی ، سختی بالا ، دمای ذوب خیلی بالا و مقاومت در برابر عوامل شیمیایی اهمیت فراوانی دارند.
نیتروژن دارای اکسیدهای متنوعی است. اکسیدهای استاندارد آن 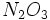 و
و  است که ناپایدار و قابل انفجار هستند.
است که ناپایدار و قابل انفجار هستند.  در آب اسید نیتریکتولید میکند که عامل اکسنده خوبی است و
در آب اسید نیتریکتولید میکند که عامل اکسنده خوبی است و 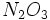 همچنین در آب اسید نیترو تولید میکند. سایر اکسیدهای نیتروژن عبارتند از :
همچنین در آب اسید نیترو تولید میکند. سایر اکسیدهای نیتروژن عبارتند از :
یکی از آلایندههای هوا است و از اگزوز اتومبیلها تولید میشود. در هوا خود بخود با 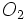 ترکیب شده و
ترکیب شده و  ایجاد میکند. همچنین از واکنش اسید نیتریکبا فلزاتی مانند مس و نقره هم ایجاد میشود.
ایجاد میکند. همچنین از واکنش اسید نیتریکبا فلزاتی مانند مس و نقره هم ایجاد میشود.
گازی قرمز یا قهوهای مایل به نارنجی است دارای بوی تندی است که تنفس آن برای انسان خطرناک است.  تمایل به دیمر شدن و ایجاد
تمایل به دیمر شدن و ایجاد  دارد.
دارد.
این گاز در دمای اتاق گازی بیرنگ و غیر قابل اشتعال است دارای بویی اندکی خوشایند بوده و در اثر تنفس آن حالت شادی و خنده به انسان دست میدهد به همین سبب به گاز خنده آور مشهور است از  در جراحی و دندانپزشکی بعنوان بیحس کننده استفاده میکنند.
در جراحی و دندانپزشکی بعنوان بیحس کننده استفاده میکنند.
آزید آنیون  است و عامل واکنشپذیر شیمی آلی در ترکیباتی که نیتروژن جایگزین کربن شده است (
است و عامل واکنشپذیر شیمی آلی در ترکیباتی که نیتروژن جایگزین کربن شده است ( 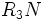 ). آزیدها معمولا ترکیباتی سمی هستند. آزیدهای آلی ترکیباتی پایدار بوده و اغلب در واکنشهای الکترو فیلی بخوبی شرکت میکنند. برخی از نمکهای معدنی آزید مانند
). آزیدها معمولا ترکیباتی سمی هستند. آزیدهای آلی ترکیباتی پایدار بوده و اغلب در واکنشهای الکترو فیلی بخوبی شرکت میکنند. برخی از نمکهای معدنی آزید مانند 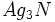 در اثر حرارت یاضربه قابلیت انفجار دارند.
در اثر حرارت یاضربه قابلیت انفجار دارند.
نیتروژن دارای دو اسید است که اسید نیتریک اسیدی قوی ، خورنده و سمی است در دمای اتاق دود زرد یا قرمز قهوهای از آن متصاعد میشود، بعنوان معرف در آزمایشگاهها و در ساخت مواد منفجره و کودهای شیمیایی در صنعت مورد استفاده قرار میگیرد. در آب تفکیک شده و H+ و یون نیترات تولید میکند. از انحلال  در آب اسید نیتریک تولید میشود. اسید نیتریک اسید ضعیف است که فقط در محلول و بصورت نمک نیتریت وجود دارد. اسید نیترو معمولا در واکنشهای ایجاد آمینها برای تولید دی آزیدها استفاده میشود.
در آب اسید نیتریک تولید میشود. اسید نیتریک اسید ضعیف است که فقط در محلول و بصورت نمک نیتریت وجود دارد. اسید نیترو معمولا در واکنشهای ایجاد آمینها برای تولید دی آزیدها استفاده میشود.
آمونیاک مهمترین ترکیب هیدروژنی است. آمونیاک اندکی خصلت بازی بیشتری نسبت به آب دارد. در آب یون آمونیوم ایجاد میکند (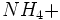 ). در دما و فشار استاندارد آمونیاک بصورت گازی با بوی تند و زننده است. در تهیه کود شیمیایی و مواد منفجره و پلیمرها استفاده میشود. امروزه آنرا با روش هابر از واکنش مستقیم
). در دما و فشار استاندارد آمونیاک بصورت گازی با بوی تند و زننده است. در تهیه کود شیمیایی و مواد منفجره و پلیمرها استفاده میشود. امروزه آنرا با روش هابر از واکنش مستقیم 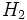 و
و 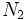 و در مجاورت کاتالیزور و دما و فشار بالا تولید میکنند.
و در مجاورت کاتالیزور و دما و فشار بالا تولید میکنند.
هیدرازین هم یکی از هیدریدهای نیتروژن به فرمول 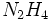 است قدرت بازی ضعیفتری نسبت به آمونیاک دارد. بعنوان سوخت موشک و همچنین در تهیه آنتی اکسیدانها و کودهای شیمیایی استفاده میشود. از اکسیداسیون آمونیاک در مجاورت هیپوکلریت سدیم حاصل میشود. تنفس آن برای سلامتی مضر بوده و باعث ایجاد سرفه و سوزش در گلو و تشنج و رعشه (اگر مدت تنفس طولانی باشد) میشود.
است قدرت بازی ضعیفتری نسبت به آمونیاک دارد. بعنوان سوخت موشک و همچنین در تهیه آنتی اکسیدانها و کودهای شیمیایی استفاده میشود. از اکسیداسیون آمونیاک در مجاورت هیپوکلریت سدیم حاصل میشود. تنفس آن برای سلامتی مضر بوده و باعث ایجاد سرفه و سوزش در گلو و تشنج و رعشه (اگر مدت تنفس طولانی باشد) میشود.
نیتراتها نمکهای نیتریک اسید هستند. نمکهای نیترات مثل پتاسیم و آمونیوم نیترات از مهمترین ترکیبات نیتروژنی مورد استفاده در صنایع حاصل خیز کننده هستند. نیترات عامل اکسنده قوی است در ترکیب با هیدروکربنها میتوانند مخلوط قابل اشتعال یا منفجر شونده ایجاد کنند.
نیتریتها نمک اسید نیترو هستند. نیتریت فلزات قلیایی و قلیایی خاکی از واکنش مخلوط NO و  با محلول هیدوکسید فلزی سنتز میشوند. نیتریتهای دیگر را از کاهش نیترات بدست میآورند. سدیم نیتریت به محصولات گوشتی اضافه میشود تا از رشد باکتریها جلوگیری کند و همچنین در اثر واکنش با پروتئین گوشت رنگ قرمز خوش رنگی به آن میبخشد به خاطر سمی بودن نیتریت میزان مجاز استفاده از آن در محصولات گوشتی ppm 200 است.
با محلول هیدوکسید فلزی سنتز میشوند. نیتریتهای دیگر را از کاهش نیترات بدست میآورند. سدیم نیتریت به محصولات گوشتی اضافه میشود تا از رشد باکتریها جلوگیری کند و همچنین در اثر واکنش با پروتئین گوشت رنگ قرمز خوش رنگی به آن میبخشد به خاطر سمی بودن نیتریت میزان مجاز استفاده از آن در محصولات گوشتی ppm 200 است.
فهرست مطالب:
آمونیاک
اهميت اقتصادي آمونياك
تولید آمونیاک
مراحل سنتز آمونیاک
تولید گاز سنتز
توليد مخلوطهاي هيدروژن، نيتروژن و كربن مونوكسيد
بازسازي با بخار آب
اكسايش جزئي مازوت (نفت كوره) سنگين
گازی کردن زغال سنگ
فرآيندهاي صنعتي براي توليد مخلوطهاي هيدروژن، نيتروژن و كربن مونوكسيد
تبدیل کربن مونوکسید
حذف CO2 و H2S
تصفيه نهايي گازهاي سنتز
كاتاليزورهاي سنتز آمونياك
مراحل توليد كاتاليزورهاي سنتز آمونياك
عوامل آلوده كننده كاتاليزورهاي سنتز آمونياك
واكنش گاز سنتز و تشكيل آمونياك
انواع رآكتور براي توليد آمونياك
جداسازی آمونیک
كارخانههاي مجتمع سنتز آمونياك
کاربردهای آمونیاک
نیتریک اسید
اصول توليد نيتريكاسيد
مرحله اول- احتراق كاتاليزوري آمونياك
مرحله دوم- اكسايش NO
مرحله سوم- تبديل نيتروژن(IV) اكسيد به نيتريكاسيد
و...


















