در شیمی معدنی ترکیباتی وجود دارند که در آن اتم مرکزی حداقل با یک پیوند داتیو با گروه اتمهای اطراف خود (لیگندها) ارتباط برقرار میکند. در این ترکیبات اتم مرکزی گیرنده جفت الکترون میباشد، چنین ترکیباتی را کمپلکس یا ترکیبات کئوردیناسیونی مینامند. اتم مرکزی در این ترکیبات معمولاً دارای یک حفره الکترونی میباشد که میتواند الکترونهای جفت نشده لیگند را بگیرد و یک پیوند کووالانسی-کئوردیناسیونی ، (داتیو) تشکیل دهد.
کمپلکسهایی که در آنها انتقال الکترون میتواند در تشکیل پیوند نقش بسزایی داشته باشد کمپلکسهای دهنده - گیرنده مینامند. اکثر عناصر جدول تناوبی اعم از فلزات گروه اصلی ، فلزات گروه واسطه و غیر فلزات میتوانند کمپلکس تشکیل دهند.
تا سال 1913 ساختمان کمپلکسها مشخص نشده بود اما در این سال آلفرد ورنر پدر شیمی کوئوردیناسیونی نظر خود را در مورد ساختمان کمپلکسها اعلام کرد و این در حالی بود که هنوز ساختمان الکترونی اتم مشخص نشده بود. قبل از ورنر دانشمندی به نام یورگنسون برای برخی از کمپلکسها ساختارهایی تعیین کرده بود که با اعلام نظریه ورنر اشتباه بودن این ساختارها مشخص شد.
ورنر به دلیل مطالعاتی که روی کمپلکسهای هشت وجهی ، مسطح مربعی و چهار وجهی انجام داد و بنیانگذار شیمی کوئوردیناسیون شد، جایزه نوبل شیمی را در سال 1913 دریافت کرد.
هر اتم دارای دو ظرفیت میباشد. ظرفیت اصلی و ظرفیت والانس فرعی ، بنابراین لزومی ندارد که فقط به اندازه ظرفیت اصلی یک اتم ، اتمهای دیگر به آن وصل شود بلکه بعد از پر شدن ظرفیت اصلی که فضای کئوردیناسیونی داخلی را تشکیل میدهد. اتمها میتوانند به ظرفیت فرعی یا فضای کئوردیناسیون خارجی که نشانگر عدد اکسیداسیون اتم مرکزی است، وارد شوند.
تا قبل از اینکه ورنر این نظریه را اعلام کند دانشمندان در تعیین ساختمان ترکیباتی مانند 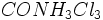 اختلاف نظر داشتند. این ترکیب یک ترکیب یونی است و کلرها در آب به راحتی یونیزه میشود. اما
اختلاف نظر داشتند. این ترکیب یک ترکیب یونی است و کلرها در آب به راحتی یونیزه میشود. اما 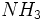 ها به آسانی جدا نمیشوند مگر اینکه ترکیب در اسید قوی جوشانده شود. یورگنسون اولین ساختمان را بر این ترکیب به صورت زیر پیشنهاد کرد.
ها به آسانی جدا نمیشوند مگر اینکه ترکیب در اسید قوی جوشانده شود. یورگنسون اولین ساختمان را بر این ترکیب به صورت زیر پیشنهاد کرد.
عکس پیدا نشد
اما ورنر این ترکیب را یک یک ساختمان هشت وجهی پیشنهاد کرد که اتم کبالت در مرکز و 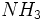 ها با شش پیوند هم اندازه در اطراف و یونهای کلر هم در فضای کئوردیناسیون خارجی حضور داشتند.
ها با شش پیوند هم اندازه در اطراف و یونهای کلر هم در فضای کئوردیناسیون خارجی حضور داشتند.
دستهای از اتمها که باهم هستند و یکی از اتمها میتواند جفت الکترونش را در اختیار اتم دیگر قرار دهد. لیگند ممکن است یک ترکیب خنثی یا یک آنیون باشد.
ترکیبات کوئوردیناسیونی که در آنها فلز مرکزی با حالت اکسایش +2 یا بالاتر توسط اتمهای غیرکربن کئوردینه شدهاند کمپلکسهای ورنر یا کلاسیک نامیده میشوند (این نامگذاری به خاطر مطالعات ورنر در شیمی کئوردیناسیون انجام شده است.).
در این کمپلکسها فلز مستقیماً با کربن پیوند تشکیل میدهد. در این ترکیبات فلز در حالت اکسایش پایین خود مانند 2- و 1- و 0 و 1+ میباشد.
در این ترکیبات اتم مرکزی گروهی از فلزات میباشند که باهم پیوند تشکیل دادهاند. مانند  که اتمهای آهن در گوشههای یک مثلث جای گرفتهاند و گروههای کربونیل در اطراف آنها پیوند تشکیل میدهند.
که اتمهای آهن در گوشههای یک مثلث جای گرفتهاند و گروههای کربونیل در اطراف آنها پیوند تشکیل میدهند.
تعداد اتمهایی که اتم مرکزی را در اولین قشر کئوردیناسیون ، کئوردینه کردهاند عدد کئوردیناسیون میگویند. عدد کئوردیناسیون هر ترکیب مشخص کننده ساختمان آن ترکیب میباشد. رایجترین عدد کئوردیناسیون در کمپلکسها عدد 6 و بعد از آن 4 میباشد.
فهرست مطالب:
رنگ کمپلکس ها
رنگ برخی از کمپلکس ها
انواع طيفهای جذبی
طيف های ليگند
طيف های يون مخالف
طيف های انتقال بار
طيف های ميدان ليگند
قواعد انتخاب
قاعده انتخاب اسپينی
جفت شدن اسپين اوربيت
قاعده انتخاب لاپورت
علل انجام انتقالات غير مجاز d-d
قانون بير - لامبرت
شدت نوارهای جذبی در کمپلکس های 3d
پهنای طيف
اثر يان - تلر در طيف الکترونی
جمله های طيفی ايجاد شده در ميدان ليگند
جمله های حاصل از آرايش dn در ميدان های ليگند هشت وجهی و چهار وجهی
ارتباط جمله های طيفی با آرايش الکترونی در ميدان هشت وجهی
بررسی طيف الکترونی در کمپلکسهای هشت وجهی d1
بررسی انتقالات الکترونی در کمپلکسهای هشت وجهی d9
نمودارهای اورگل
بررسی انتقالات الکترونی در کمپلکسهای هشت وجهی d6
بررسی انتقالات الکترونی در کمپلکسهای هشت وجهی d5
مقايسه نمودارهای تراز انرژی در ميدانهای هشت وجهی و چهار وجهی
پارامترهای راکا
اثر انبساط ابر الکترونی (اثر نفلاکستی)
نمودارهای تانابه - سوگانو
تفسير طيف الکترونی کمپلکسها
تفاوتهای طيف الکترونی کمپلکسهای d5 با طيف الکترونی ساير کمپلکسها
ويژگيهای طيف های انتقال بار
جهشهای انتقال بار در کمپلکسهای هشت وجهی
جهشهای انتقال بار و واکنش های اکسايش - کاهش
کمپلکسهای ظرفيت مختلط
طيف الکترونی کمپلکسهای لانتانيدی
طيف الکترونی کمپلکسهای آکتينيدی
انواع طيف های آکتينيدی
خواص مغناطيسی کمپلکسهای فلزی
مواد ديامغناطيس
مواد پارامغناطيس
نفوذپذيری مغناطيسی مولی برخی مواد
اثر دما در نفوذپذيری مغناطيسی
ممان مغناطيسی اسپينی و اوربيتالی
روش گوی برای تعيين نفوذپذيری مغناطيسی
عوامل موثر در رفتار پارامغناطيسی يک يون
انواع کمپلکسهای يونی از نظر رفتار پارامغناطيسی
تعيين آرايش الکترونی کمپلکسها با استفاده از ممان مغناطيسی
سهم اوربيتالی ممان مغناطيسی
و...




